
Fermium
Saviez-vous ...
SOS Enfants, un organisme de bienfaisance de l'éducation , a organisé cette sélection. SOS Enfants a regardé des enfants en Afrique depuis quarante ans. Pouvez-vous aider dans leur travail en Afrique ?
| Fermium | |||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
100 Fm | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| Apparence | |||||||||||||||||||||||||||||||||||||||||||
| inconnu | |||||||||||||||||||||||||||||||||||||||||||
| Propriétés générales | |||||||||||||||||||||||||||||||||||||||||||
| Nom, symbole, nombre | fermium, Fm, 100 | ||||||||||||||||||||||||||||||||||||||||||
| Prononciation | / fa ɜr m Je ə m / FER -mee-əm | ||||||||||||||||||||||||||||||||||||||||||
| Élément Catégorie | actinides | ||||||||||||||||||||||||||||||||||||||||||
| Groupe, période, bloc | n / a, 7, fa | ||||||||||||||||||||||||||||||||||||||||||
| Poids atomique standard | (257) | ||||||||||||||||||||||||||||||||||||||||||
| Configuration électronique | [ Rn ] 5f 12 7s 2 2, 8, 18, 32, 30, 8, 2  | ||||||||||||||||||||||||||||||||||||||||||
| Histoire | |||||||||||||||||||||||||||||||||||||||||||
| Découverte | Lawrence Berkeley National Laboratory (1952) | ||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques | |||||||||||||||||||||||||||||||||||||||||||
| Phase | solide | ||||||||||||||||||||||||||||||||||||||||||
| Point de fusion | 1800 K , 1527 ° C, 2781 ° F | ||||||||||||||||||||||||||||||||||||||||||
| Propriétés atomiques | |||||||||||||||||||||||||||||||||||||||||||
| États d'oxydation | 2, 3 | ||||||||||||||||||||||||||||||||||||||||||
| Électronégativité | 1,3 (échelle de Pauling) | ||||||||||||||||||||||||||||||||||||||||||
| énergies d'ionisation | 1er: 627 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||
| Miscellanées | |||||||||||||||||||||||||||||||||||||||||||
| Numéro de registre CAS | 7440-72-4 | ||||||||||||||||||||||||||||||||||||||||||
| La plupart des isotopes stables | |||||||||||||||||||||||||||||||||||||||||||
| Article détaillé: Isotopes de fermium | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
Fermium est un élément synthétique avec le symbole Fm et de numéro atomique 100. Ce est un membre de l' actinide série. Ce est l'élément le plus lourd qui peut être formé par neutrons bombardement d'éléments plus légers, et donc le dernier élément qui peut être préparé en quantités macroscopiques, bien fermium métal pur n'a pas encore été établie. Un total de 19 isotopes sont connus, avec 257 Fm étant la plus longue durée de vie un avec une demi-vie de 100,5 jours.
Il a été découvert dans les débris de la première bombe hydrogène explosion en 1952, et nommé d'après Lauréat du prix Nobel Enrico Fermi, l'un des pionniers de la physique nucléaire . Sa composition chimique est typique de la fin des actinides, avec une prépondérance de la 3 état d'oxydation , mais aussi un état d'oxydation +2 accessible. En raison des petites quantités de fermium produit et sa demi-vie courte, il n'y a actuellement aucune utilisation pour elle en dehors de la recherche scientifique fondamentale. Comme tous les éléments synthétiques, isotopes de fermium sont extrêmement radioactifs et sont considérés comme très toxiques.
Découverte


Fermium a été découvert dans les retombées de la ' Test Ivy Mike 'nucléaire (1 Novembre 1952), le premier essai réussi d'une bombe à hydrogène. L'examen initial des débris de l'explosion a montré la production d'une nouvelle isotope de plutonium , 244
94 Pu: ce ne pouvait être formé par l'absorption des six neutrons par un l'uranium-238 noyau suivie de deux β - se désintègre. À l'époque, l'absorption des neutrons par un noyau lourd a été pensé pour être un processus rare, mais l'identification des 244
94 Pu soulevé la possibilité que toujours plus de neutrons auraient pu être absorbée par les noyaux d'uranium, menant à de nouveaux éléments.
Element 99 ( einsteinium ) a été rapidement découvert sur du papier filtre qui avait été volé à travers le nuage de l'explosion (la même technique d'échantillonnage qui avait été utilisé pour découvrir 244
94 Pu). Il a ensuite été identifié en Décembre 1952 par Albert Ghiorso et co-travailleurs de la Université de Californie à Berkeley. Ils ont découvert l'isotope 253 Es ( demi-vie 20,5 jours) qui a été faite par le 15 capture de neutrons par uranium-238 noyaux - qui a ensuite subi sept successive désintégrations bêta:
Quelques 238 atomes U, cependant, pourraient capturer une autre quantité de neutrons (le plus probable, 16 ou 17).
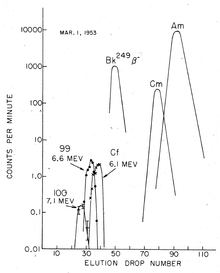
La découverte de fermium (Z = 100) requis plus de matériel, comme devait le rendement à au moins un ordre de grandeur inférieur à celui de l'élément 99, et ainsi contaminé corail de la Enewetak Atoll (où le test a eu lieu) a été expédié à la Université de Californie Radiation Laboratory dans Berkeley, en Californie, pour traitement et analyse. Environ deux mois après le test, un nouveau composant a été isolé émettant à haute énergie α-particules (7,1 MeV) avec une demi-vie d'environ un jour. Avec un tel demi-vie courte, il ne pouvait découler de la β - désintégration d'un isotope de l'einsteinium, et devaient donc être un isotope de l'élément nouveau 100: il a été rapidement identifié comme 255 Fm (t ½ = 20,07 (7 ) heures).
La découverte de nouveaux éléments, et les nouvelles données sur la capture de neutrons, a d'abord été gardés secrets sur les ordres de l'armée américaine jusqu'en 1955 en raison de la guerre froide tensions. Néanmoins, l'équipe de Berkeley ont pu préparer des éléments 99 et 100 par des moyens civils, à travers le bombardement de neutrons des plutonium 239, et publié ce travail en 1954 avec l'avertissement qu'il ne était pas les premières études qui ont été menées sur les éléments. Les études «Ivy Mike 'ont été déclassifiés et publiés en 1955.
L'équipe de Berkeley avait été inquiet qu'un autre groupe puisse découvrir isotopes les plus légers de l'élément 100 par le biais de techniques de bombardement ionique avant qu'ils puissent publier leurs recherches classifiées, et cela se est avéré être le cas. Un groupe à l'Institut Nobel de physique à Stockholm découvert indépendamment l'élément, la production d'un isotope confirmé plus tard pour être 250 Fm (t ½ = 30 minutes) en bombardant une 238
92 U cible avec oxygène 16 ions, et publié leur travaux en mai 1954. Néanmoins, la priorité de l'équipe de Berkeley a été généralement reconnu, et avec elle la prérogative de nommer le nouvel élément en l'honneur du récemment décédé Enrico Fermi, le développeur du premier réacteur nucléaire auto-entretenue artificielle.
Isotopes

Il ya 19 isotopes de fermium énumérés dans N UBASE 2003, avec des poids atomiques de 242 à 260, dont 257 Fm est le plus long-vécu avec une demi-vie de 100,5 jours. Fm 253 a une demi-vie de 3 jours, tandis que 251 Fm de 5,3 h, 252 Fm de 25,4 h, 254 Fm de 3,2 h, 255 Fm de 20,1 h, et 256 Fm de 2,6 heures. Tous les restants ont des demi-vies allant de 30 minutes à moins d'une milliseconde. Le produit de la capture de neutrons fermium-257, 258 Fm, subit fission spontanée avec une demi-vie de seulement 370 microsecondes (14); 259 et 260 Fm Fm sont également instable par rapport à la fission spontanée (t ½ = 1,5 (3) s et 4 ms respectivement). Cela signifie que la capture de neutrons ne peut pas être utilisé pour créer nucléides avec un nombre de masse supérieure à 257, sauf réalisée dans une explosion nucléaire. Comme 257 Fm est un α-émetteur, en décomposition à 253 Cf, et aucun isotopes de fermium subissent désintégration bêta moins (ce qui serait de produire des isotopes de l'élément suivant, mendelevium), fermium est aussi le dernier élément qui peut être préparé par un procédé capture de neutrons.
Production
Fermium est produite par le bombardement de légers actinides avec des neutrons dans un réacteur nucléaire. Fermium-257 est l'isotope le plus lourd qui est obtenue par capture de neutrons, et ne peut être produite en quantités de l'ordre du nanogramme. La source principale est le 85 MW High Flux Isotope Reactor (HFIR) au Oak Ridge National Laboratory Tennessee, Etats-Unis, qui se consacre à la production de transcurium (Z> 96) éléments. Dans une "campagne de traitement typique» à Oak Ridge, des dizaines de grammes de curium sont irradiés pour produire des quantités de decigramme de californium , les quantités de milligrammes de berkelium et einsteinium et des quantités de l'ordre du picogramme fermium. Cependant, des quantités de l'ordre du microgramme et fermium nanogramme peuvent être préparés pour des expériences spécifiques. Les quantités de fermium produit dans 20 à 200 kilotonnes explosions thermonucléaires on croit être de l'ordre de milligrammes, même se il est mélangé avec une énorme quantité de débris; 40 257 picogrammes d'Fm a été récupéré à partir de 10 kg de débris de la ' Test Hutch »(16 Juillet 1969).
Après la production, la fermium doit être séparé des autres actinides et de lanthanides produits de fission. Ceci est habituellement réalisé par Chromatographie d'échange d'ions, le procédé standard en utilisant un échangeur de cations Dowex 50 tel que l'EVA ou T éluée avec une solution d'α-hydroxyisobutyrate d'ammonium. Les petits cations forment des complexes plus stables avec l'anion α-hydroxyisobutyrate, et ainsi sont de préférence éluées de la colonne. Un rapide Procédé de cristallisation fractionnée a également été décrite.
Bien que l'isotope le plus stable de fermium est 257 Fm, avec une demi-vie de 100,5 jours, la plupart des études sont effectuées sur 255 Fm (t ½ = 20,07 (7) heures) comme cet isotope peut être facilement isolé selon les besoins comme le produit de désintégration 255 Es (t ½ = 39,8 (12) jours).
Synthèse des explosions nucléaires
L'analyse des débris à la 10- mégatonnes Ivy Mike essai nucléaire était une partie de projet à long terme, l'un des objectifs qui a été étudient l'efficacité de la production d'éléments transuraniens dans les explosions nucléaires à haute puissance. La motivation de ces expériences était comme suit: synthèse de ces éléments de l'uranium nécessite capture de neutrons multiple. La probabilité de tels événements augmente avec le flux de neutrons, et les explosions nucléaires sont les sources les plus puissants de neutrons, fournir des densités de l'ordre de 10 23 neutrons / cm² dans une microseconde, soit environ 10 29 neutrons / (cm² · s). En comparaison, le flux du réacteur est HFIR 5 x 10 15 neutrons / (cm² · s). Un laboratoire spécialisé a été mis en place à droite au Enewetak Atoll pour l'analyse préliminaire des débris, comme certains isotopes auraient pourri au moment où les échantillons de débris a atteint les Etats-Unis Le laboratoire recevait des échantillons pour analyse, dès que possible, à partir d'avions équipés de filtres en papier qui ont survolé l'atoll après les essais . Considérant qu'il espérait découvrir de nouveaux éléments chimiques plus lourds que fermium, ceux qui ne ont pas été trouvé après une série d'explosions de mégatonnes menée entre 1954 et 1956 sur l'atoll.
Les résultats atmosphériques ont été complétées par les données de test souterraines accumulées dans les années 1960 à la Nevada Test Site, car il est à espérer que de puissantes explosions menées dans un espace confiné peut aboutir à des rendements améliorés et des isotopes plus lourds. Outre les accusations d'uranium traditionnelles, des combinaisons de l'uranium et du thorium avec américium ont été essayées, ainsi qu'une charge de plutonium neptunium mixte. Ils étaient moins de succès en termes de rendement qui a été attribué à des pertes plus fortes d'isotopes lourds en raison de l'amélioration des taux de fission dans charges éléments lourds. Isolement des produits a été jugée assez problématique, que les explosions se répandaient débris à travers la fusion et de vaporisation des roches sous la grande profondeur de 300 à 600 mètres, et le forage à la profondeur afin d'en extraire les produits était à la fois lent et inefficace en termes des volumes collectés.
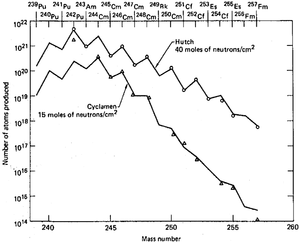
Parmi les neuf essais souterrains, qui ont été réalisées entre 1962 et 1969 et le nom de code Anacostia (5.2 kilotonnes, 1962), Kennebec (<5 kilotonnes, 1963), Par (38, kilotonnes, 1964), le barbeau (<20 kilotonnes, 1964), Tweed (<20 kilotonnes, 1965), Cyclamen (13 kilotonnes, 1966), Kankakee (de 20 à 200 kilotonnes, 1966), Vulcan (25 kilotonnes, 1966) et Hutch (20-200 kilotonnes, 1969), la dernière était la plus puissante et avait le meilleur rendement des éléments transuraniens. En fonction du nombre de masse atomique, le rendement a montré un comportement en dents de scie avec des valeurs plus faibles pour les isotopes impairs, en raison de leur taux de fission plus élevés. Le problème pratique majeur de l'ensemble de la proposition a toutefois été recueille les débris radioactifs dispersés par le souffle puissant. filtres d'aéronefs adsorbées seulement environ 4 × 10 -14 du montant total et la collecte de tonnes de coraux à Enewetak Atoll augmenté cette fraction par seulement deux ordres de grandeur. Extraction d'environ 500 kg de roches souterraines 60 jours après l'explosion Hutch récupéré seulement environ 10 -7 de la charge totale. La quantité d'éléments transuraniens de ce lot de 500 kg ne était que de 30 fois plus élevé que dans un 0,4 kg de roche ramassé sept jours après le test. Cette observation a démontré la dépendance fortement non linéaire de la transuraniens donnent sur le montant de la roche radioactive récupérée. Afin d'accélérer la collecte de l'échantillon après l'explosion, des arbres ont été forés sur le site pas après, mais avant le test, de sorte que l'explosion serait expulser matières radioactives de l'épicentre, à travers les arbres, à la collecte de volumes près de la surface. Cette méthode a été jugé dans les tests Anacostia et Kennebec et instantanément fourni des centaines de kilogrammes de matériel, mais avec une concentration des actinides trois fois plus faible que dans les échantillons obtenus après le forage; que cette méthode aurait pu être efficace dans des études scientifiques d'isotopes de courte durée, il ne pouvait pas améliorer l'efficacité globale de la collecte des actinides produits.
Bien qu'aucune de nouveaux éléments (à l'exception de einsteinium et fermium) pourraient être détectés dans les débris des essais nucléaires, et les rendements totaux des transuraniens étaient décevants, ces tests ne fournissent des quantités significativement plus élevées d'isotopes lourds rares qu'auparavant disponibles dans les laboratoires. Donc 6 × 10 9 atomes de 257 Fm pourraient être récupérés après la détonation Hutch. Ils ont ensuite été utilisées dans les études de neutrons thermiques scission induite de 257 Fm et à la découverte d'un nouvel isotope de fermium 258 Fm. Aussi rare 250 cm isotope a été synthétisé en grandes quantités, ce qui est très difficile de produire dans les réacteurs nucléaires de son ancêtre 249 cm - la demi-vie de 249 cm (64 minutes) est beaucoup trop court pour des irradiations de réacteurs mois-longues, mais est très "long" sur le calendrier d'explosion.
Occurrence naturelle
En raison de la courte demi-vie de tous les isotopes de l'fermium, toutes fermium primordial, ce est-fermium qui pourraient être présents sur la Terre lors de sa formation, est désintégrée par l'entreprise. Synthèse des actinides fermium de l'uranium et du thorium naturel dans la croûte terrestre nécessite multiple capture de neutrons, ce qui est un cas extrêmement improbable. Par conséquent, la plupart fermium est produite sur Terre dans les laboratoires scientifiques, les réacteurs nucléaires de forte puissance, ou dans essais d'armes nucléaires, et ne est présent que dans quelques mois à partir du moment de la synthèse. Einsteinium et fermium ne se produisent naturellement dans le naturelle réacteur de fission nucléaire à Oklo, mais ne est plus le faire.
Chimie
La chimie de fermium n'a été étudié en solution en utilisant des techniques de traçage, et aucun des composés solides ont été préparés. Dans des conditions normales, fermium existe en solution sous forme d'ion Fm 3+, qui présente un certain nombre d'hydratation de 16,9 et un constante de dissociation acide de 1,6 × 10 -4 (p K a = 3,8). Fm 3+ formant des complexes avec une grande variété de ligands organiques avec des atomes donneurs durs, tels que l'oxygène, et ces complexes sont généralement plus stables que ceux des actinides précédentes. Il forme également des complexes anioniques avec des ligands tels que le chlorure ou le nitrate et, encore une fois, ces complexes semblent être plus stables que ceux formés par einsteinium ou californium . On pense que la liaison dans les complexes des actinides ultérieures est surtout ionique de caractère: l'ion Fm 3+ devrait être plus petite que les précédentes Un 3+ ions en raison de la plus élevée charge nucléaire effective de fermium, et donc fermium serait prévu pour former des liaisons plus courtes et plus fortes métal-ligand.
Fermium (III) peut être assez facilement réduit à fermium (II), par exemple avec samarium (II) chlorure, avec lequel fermium coprécipités. Le potentiel de l'électrode a été estimée être similaire à celle de l' ytterbium (III) / (II) en couple, ou environ -1,15 V par rapport à la électrode à hydrogène standard, une valeur qui est en accord avec les calculs théoriques. Le Fm 2+ / Fm 0 couple a un potentiel d'électrode de -2,37 (10) V sur la base mesures polarographiques.
Toxicité
Bien que peu de gens viennent en contact avec fermium, le Commission internationale de protection radiologique a fixé des limites annuelles d'exposition pour les deux isotopes les plus stables. Pour fermium-253, la limite de l'ingestion a été fixé à 10 7 Becquerels (Bq 1 équivaut à une désintégration par seconde), et la limite d'inhalation à 10 5 Bq; pour fermium-257, à 10 Bq 5 et 4000 Bq respectivement.

